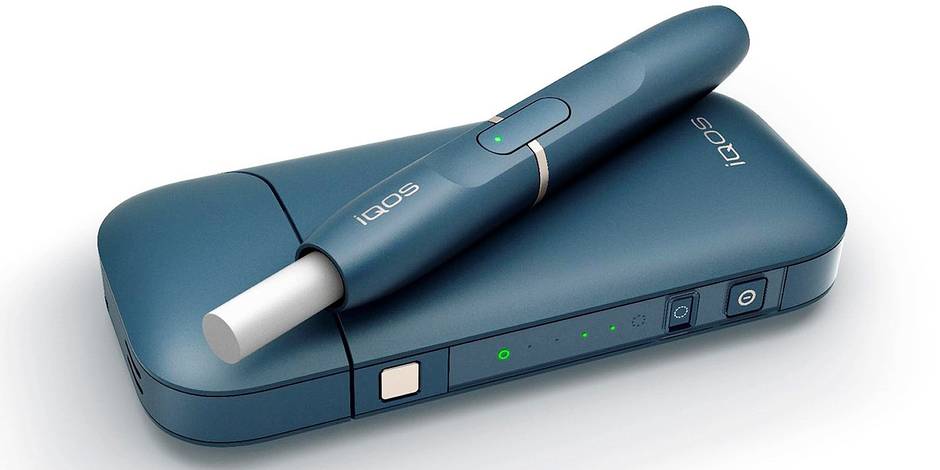
Juul Labs domine actuellement le marché américain des cigarettes électroniques avec une part de 75%, alors que Philip Morris International (NYSE:PM) en détient actuellement 0%. Mais si les choses se passent bien pour Philip Morris au cours des deux prochaines années environ, ces positions pourraient être complètement inversées.
Le géant mondial du tabac est sur le point d’introduire sur le marché américain son appareil à tabac chauffé IQOS. Les ventes seront probablement soutenues si l’expérience de Philip Morris International sur d’autres marchés est une indication de la façon dont elle sera reçue ici. De plus, compte tenu de l’environnement réglementaire actuel, il semble fort probable que Philip Morris et son partenaire domestique, Altria Group (NYSE : MO), deviendront rapidement propriétaires du marché.
Les petits fabricants de cigares électroniques peuvent être anéantis par les contraintes financières de la conformité.
Aucun grand fabricant n’a indiqué qu’il était prêt à respecter l’échéance.
Juul, le leader du marché, semble être trop populaire auprès des adolescents pour répondre aux exigences réglementaires.
Avec toute la concurrence paralysée, IQOS pourrait très bien devenir le seul e-cig sur le marché. Alors que les détracteurs de la réglementation de la FDA sur la cigarette électronique appelaient le « Big Tobacco Protection Act », peu d’entre eux prévoyaient sans doute que l’agence allait créer ce qui pourrait devenir un monopole de la cigarette électronique.
Le lève-tôt prend le dessus
Donnez du crédit à Philip Morris International. Contrairement à ses concurrents, le géant mondial du tabac n’a pas attendu pour soumettre une demande de commercialisation à la FDA. Il a agi immédiatement.
En décembre 2016, elle a présenté sa demande de produits du tabac à risque modifié pour qu’IQOS puisse la commercialiser comme étant plus sécuritaire que les cigarettes et, trois mois plus tard, elle a présenté sa demande de produits du tabac précommercialisation (PMTA) pour examen. La PMTA est exigée de tous les fabricants de cigarettes électroniques et doit être révisée et approuvée par la FDA avant que tout nouveau produit du tabac puisse être légalement vendu aux États-Unis. Fin avril, la FDA a donné à Philip Morris le droit de vendre IQOS, tout en retardant l’approbation de l’affirmation de Philip Morris selon laquelle le produit est plus sûr que les cigarettes traditionnelles.
Entre-temps, avec d’autres fabricants de cigarettes électroniques, l’agence a d’abord reporté la date limite de conformité jusqu’en 2022 (et l’a ensuite reportée à 2021 plus tôt cette année) et a permis que de nouveaux produits soient mis sur le marché sans examen. Les militants antitabac ont accusé l’agence d’avoir violé sa responsabilité de réglementer les appareils et ont intenté une poursuite devant la cour fédérale pour forcer la FDA à agir. Le juge dans l’affaire a accepté et, le mois dernier, a demandé à la FDA de présenter un plan pour réglementer les fabricants de cigares électroniques.
La FDA a offert un délai de 10 mois pour la soumission des ACTP ; les groupes antitabac veulent un délai de six mois. Les deux permettront aux dispositifs de demeurer sur le marché pendant un an en attendant l’examen de leurs demandes par l’agence.
Un processus complexe et coûteux
Le problème pour les fabricants de e-cig est que l’application n’est pas un simple document de deux pages. La demande de Philip Morris aurait fait plus d’un million de pages et coûté des millions de dollars à produire. Les petits fabricants n’auront tout simplement pas les ressources financières nécessaires pour se conformer aux règles complexes qui les empêchent de retirer leurs produits du marché.
Les grands fabricants ont les ressources nécessaires pour répondre aux exigences onéreuses, mais ils ne l’ont pas encore fait. British American Tobacco (NYSE : BTI) a déclaré qu’elle était prête à soumettre sa PMTA avant l’échéance de 2021, mais la fermeture rapide de la fenêtre de conformité pourrait rendre cette tâche plus difficile.
Pourtant, même si les compagnies de tabac américaines britanniques ou d’autres compagnies de tabac soumettent en fin de compte une LEMP, l’attente peut être longue avant d’obtenir l’approbation. L’agence dit qu’elle vise à prendre une décision sur une demande dans les six mois suivant sa réception, mais qu’il a fallu plus de deux ans à la FDA pour approuver IQOS, et l’évaluation à risque réduit de Philip Morris est toujours en cours. Même s’il n’y a pas un déluge de demandes à la date limite, l’agence pourrait mettre beaucoup de temps à les régler.
Nulle part ailleurs où se tourner
Juul et Altria sont dans une situation particulière. Altria a payé 12,8 milliards de dollars pour une participation de 35 % dans le principal fabricant de cigares électroniques, mais Juul fait l’objet d’un examen minutieux en raison de son utilisation présumée par des adolescents. L’ancien commissaire de la FDA Scott Gottlieb doutait que le dispositif soit approuvé à cause de cela.
Cela signifie que l’IQOS pourrait être la seule cigarette électronique qui reste en place après l’expiration du délai prévu par la LEMP et la période d’attente pour l’intervention de l’organisme est passée et est passée.
Cela confère à Altria une position particulière car elle a le potentiel de bénéficier à la fois de Juul et d’IQOS en tant que deux des plus grandes marques sur le marché. Même si les scénarios apocalyptiques se réalisent, Altria aura toujours le droit de commercialiser IQOS.
Avec plusieurs années de succès commercial à son actif grâce à la vente d’IQOS dans d’autres pays, Philip Morris a des raisons de croire que sa plateforme de chauffage au tabac sera un grand succès sur le marché américain. C’est une bonne nouvelle pour Philip Morris et Altria, et même si un rival parvient à traverser le labyrinthe réglementaire, IQOS aura une longueur d’avance pour dominer le marché du e-cig.
NuMedia est un média indépendant. Soutiens-nous en nous ajoutant à tes favoris sur Google Actualités :